آزمایش Tumor Profiling
جهشهای ژنتیکی در بافت تومور یکی از مهمترین بیومارکرهای تومور هستند که برای تشخیص نوع سرطان، طبقهبندی آن، تخمین پیشآگهی و انتخاب درمان مناسب از اهمیت بسیاری برخوردار میباشند. آزمایش تعیین پروفایل ژنتیکی تومور ( Tumor Profiling نوع یک ) روش تشخیص آزمایشگاهی بر پایه توالییابی نسل جدید است که با مشخص کردن جهشهای ژنتیکی سلولهای سرطانی که برای آنها داروی مشخصی وجود دارد، امکان درمان مؤثرتر سرطان را فراهم میآورد. برخی از ژنهای مورد بررسی در این آزمایش همچنین در دستهبندی نوع سرطان و یا تعیین پیش آگهی آن کاربرد دارند. آزمایش Tumor Profiling نوع یک بر روی DNA جدا شده از نمونه ﺑﻠﻮکهای ﺑﺎﻓت ﭘﺎراﻓﯿﻨﻪ و ﻓﯿﮑﺲ ﺷـﺪه ﺑـﺎ ﻓﺮﻣـﺎﻟﯿن (FFPE) انجام میشود. این آزمایش به عنوان یک روش تشخیصی کمکی به حساب میآید تا بیمارانی که ممکن است از درمانهای هدفمند (Targeted Therapy) بهرهمند شوند، را شناسایی کند.
در آزمایش تعیین پروفایل ژنتیکی تومور نوع دو با استفاده از توالییابی نسل جدید، جهشهای ژنتیکی در بیش از ۵۰ ژن با اهمیت بالینی در درمان سرطانهای مختلف، وضعیت MSI (mircosatellite instability) و TMB (tumor mutation burden) در بافت تومور تعیین میشود. جهت اطلاع از آزمایش MSI کلیک کنید. به علاوه در این آزمایش ۴۷ ژن مرتبط با سرطانهای وراثتی در نمونه خون بررسی میشود. در آزمایش Tumor profiling نوع دو هر دو نمونه تومور و نمونه خون بیمار بررسی میشود.
آزمایش TMB
TMB (Tumor Mutation Burden) بر اساس تعداد جهشهای سوماتیک در ناحیه کد کننده ژنوم تومور تعریف میشود و مارکر بالینی جدیدی برای پاسخ به ایمونوتراپی محسوب میشود. High TMB (TMB-H) ، ≥10 موتاسیون در هر مگاباز DNA، با افزایش بیان نئوآنتی ژنهای اختصاصی تومور همراهی دارد که بخشی از آنها توسط سیستم ایمنی قابل شناسایی هستند.
در آزمایش تعیین پروفایل ژنتیکی تومور نوع ۳ با استفاده از توالییابی نسل جدید، جهشهای ژنتیکی در ۱۹ ژن با اهمیت بالینی در درمان سرطانهای مختلف، در بافت تومور تعیین میشود. ژنهای مورد بررسی در این آزمایش در انتخاب درمان موثر، دستهبندی نوع سرطان و تعیین پیش آگهی آن کاربرد دارند. آزمایش Tumor Profiling نوع ۳ بر روی DNA جدا شده از نمونه بلوکهای بافت پارافینه و فیکس شده با فرمالین (FFPE) انجام میشود. این آزمایش به عنوان یک روش تشخیصی کمکی به حساب میآید تا بیمارانی که ممکن است از درمانهای هدفمند (Therapy Targeted) بهرهمند شوند، را شناسایی کند.

ژنها و جهشهای مورد بررسی در آزمایش Tumor Profiling ۱
آزمایش Tumor Profiling
نوع یک
با استفاده از جدیدترین تکنولوژیهای آزمایشگاهی و آنالیز داده روز
دنیا، علاوه بر تعیین جهشهای تک نوکلئوتیدی و حذف یا اضافههای کوچک در ۴۰ ژن مرتبط با پیشرفت
سرطان، امکان بررسی افزایش تعداد کپیهای ۸ ژن و وجود محصولات فیوژنی ۹ ژن با اهمیت بالینی را
فراهم میآورد.
تغییرات تک نوکلئوتیدی (SNV):
با استفاده از بارکدهای مولکولی در تهیه کتابخانه رشتههای DNA مورد استفاده در این آزمایش، امکان شناسایی جهشهای با فراوانی ۱% میسر گردیده است. تمامی ۲۲ جهش با فراوانی ۴% موجود در نمونه DNA تومور کنترل شرکت SeraCare با استفاده از آزمایش Tumor Profiling نوع یک به درستی تشخیص داده شد.
تغییرات تعداد کپی ژن (CNV):
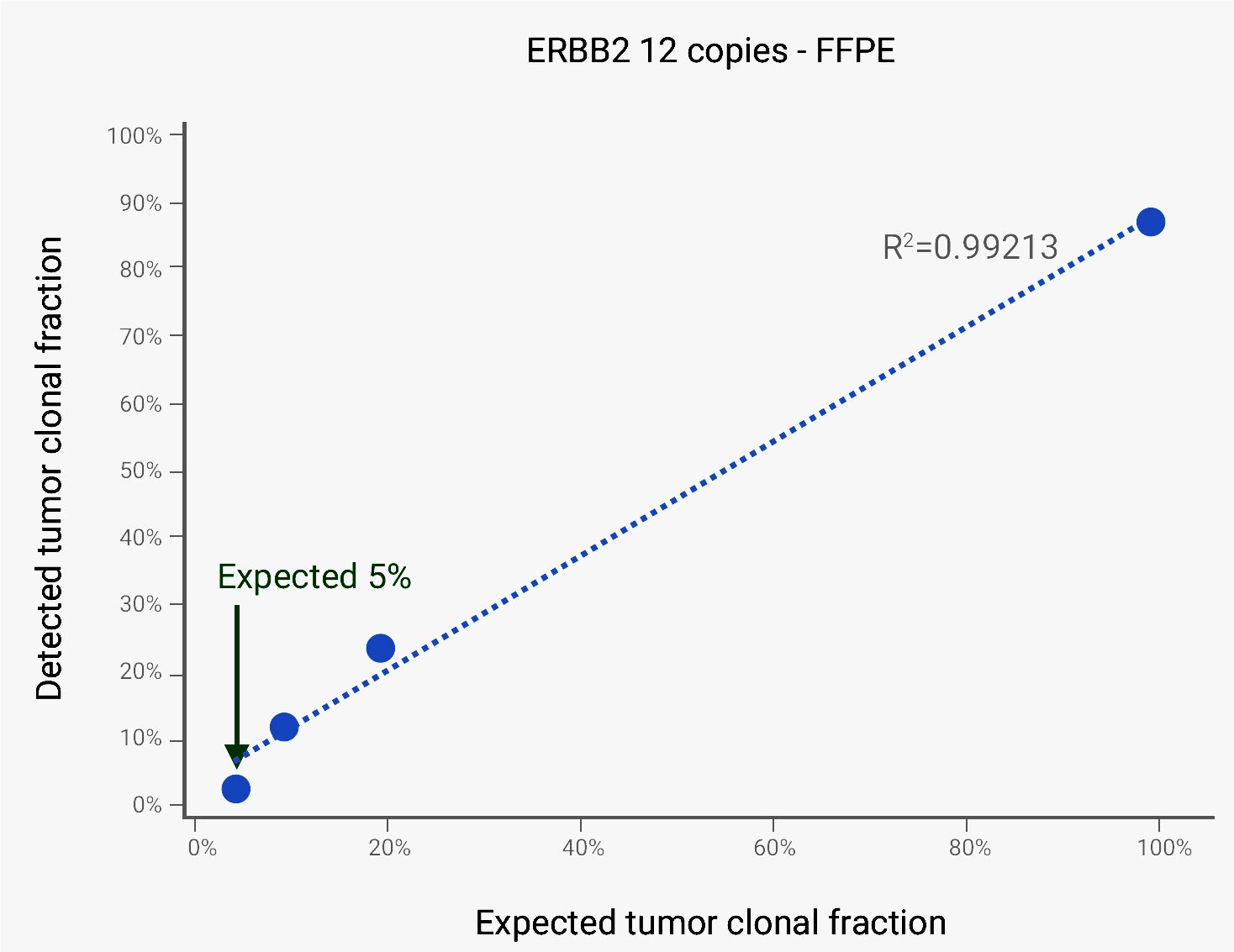
در این آزمایش علاوه بر ژنهای مورد بررسی، ۱۰۰Kbp از ژنوم به عنوان کنترل در هر نمونه توالییابی میشود، تا امکان تعیین کم یا اضافه شدن کپیهای یک ژن در سلولهای سرطانی تا نسبت کلونی ۱۵-۱۰% میسر گردد. در یک نمونه FFPE تومور پستان دارای ۱۲ کپی از ژن ERBB2، افزایش تعداد کپیهای این ژن در نمونه های DNA رقیق شده به نسبت ۱۰۰%، ۲۰% و ۱۰% با آزمایش Tumor Profiling نوع یک به درستی تعیین گردید. همچنین تعداد کپیهای ژن ERBB2 در ۵ نمونه FFPE تومور پستان تعیین شده با آزمایش Tumor Profiling نوع یک ، با تعداد کپیهای اندازه گیری شده با FISH مطابقت خوبی داشت.
| نمونه تومور | تعداد کپیهای ERBB2 با FISH | تعداد کپیهای ERBB2 با Tumor Profiling نوع یک |
|---|---|---|
| بلوک FFPE شماره ۱ | ۱۰/۲ | ۱۵ |
| بلوک FFPE شماره ۲ | ۶/۲ | ۵ |
| بلوک FFPE شماره ۳ | ۸ | ۱۴ |
| بلوک FFPE شماره ۴ | ۸/۴ | ۸ |
| بلوک FFPE شماره ۵ | ۱۰ | ۱۵ |
فیوژن (Translocation):
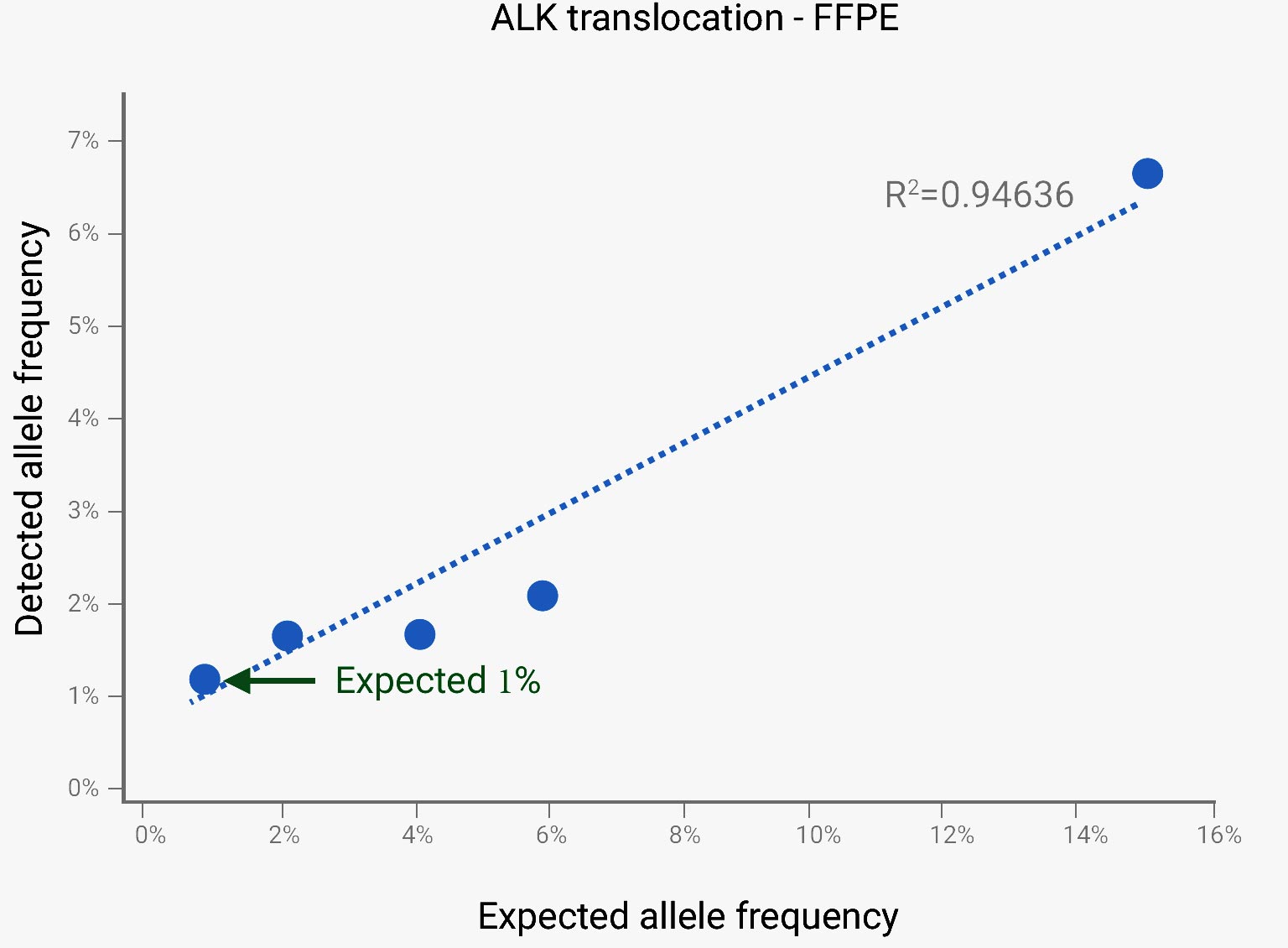
با استفاده از طراحی ویژه پروبهای شرکت Agilent و آنالیز پیشرفته دادهها در آزمایش Tumor Profiling نوع یک ، امکان تشخیص Translocation در سلولهای سرطانی تا نسبت کلونی ۱% فراهم گردیده است. یک نمونه DNA تومور دارای Translocation بین ژنهای ALK و EML4 به نسبتهای ۱۰۰%، ۶%، ۴%، ۲% و ۱% رقیق شده و آزمایش Tumor Profiling نوع یک با دقت خوبی Translocation ژن ALK را در تمام نمونهها شناسایی نمود.
فهرست ژنها و نوع جهشهای مورد بررسی آنها در آزمایش Tumor Profiling نوع یک
| نام ژن | تغییرات تک نوکلئوتیدی (SNV) | تغییرات تعداد کپی ژن (CNV) | فیوژن (Translocation) |
|---|---|---|---|
| ABL1 | |||
| ALK | |||
| AR | |||
| ATM | |||
| BRAF | |||
| BRCA1 | |||
| BRCA2 | |||
| CD274 (PD-L1) | |||
| CDK4 | |||
| CDKN2A | |||
| EGFR | |||
| ERBB2 | |||
| ESR1 | |||
| FGFR2 | |||
| FGFR3 | |||
| IDH1 | |||
| IDH2 | |||
| KIT | |||
| KRAS | |||
| MDM2 | |||
| MET | |||
| MLH1 | |||
| MSH2 | |||
| MSH6 | |||
| NF1 | |||
| NRAS | |||
| NTRK1 | |||
| NTRK2 | |||
| NTRK3 | |||
| PDGFRA | |||
| PIK3CA | |||
| PMS2 | |||
| RET | |||
| ROS1 | |||
| SMARCB1 | |||
| SMO | |||
| TERT | |||
| TP53 | |||
| TSC1 | |||
| VHL |
کاربردهای بالینی نمونهای از ژنهای مورد بررسی در آزمایش Tumor Profiling نوع یک
فیوژن این ژن با ژنهای دیگر که بیشتر در سرطان ریه غیر سلول کوچک (NSCLC) دیده میشود، پیشبینی کننده پاسخ به درمان با مهار کنندههای ALK تیروزین کیناز (ALK TKI) مثل Alektinib، Crizotinib و Brigatinib میباشد. همچنین وجود جهشهای فعالکننده ALK در نوروبلاستوما، با پیش آگهی بد ارتباط داشته و پیشبینی کننده پاسخ یا عدم پاسخ به درمان با مهار کنندههای ALK تیروزین کیناز (ALK TKI) مثل Crizotinib میباشد.
وجود جهشهای BRAF به طور شایعی در سرطانهای ملانوما، کولون، ریه غیر سلول کوچک (NSCLC)، تیرویید، پستان و گلیومای بد خیم دیده میشود. سرطانهای کولون دارای جهشهای BRAF پاسخ کاهش یافته به داروهای Cetuximab، Vemurafininb و Panitumumab داشته و تومورهای استرومای دستگاه گوارش (GIST) دارای جهش در ژن BRAF مقاوم به داروهای Imatinib و Sunitinib میباشند. همچنین داروهای Dabrafenib، Dasatinib، Trametinib و Vemurafenib در ملانوما و سرطان ریه غیر سلول کوچک (NSCLC) دارای جهشهای BRAF مورد استفاده دارند.
وجود جهشهای BRCA1/2 به طور شایعی در سرطانهای ریه غیر سلول کوچک (NSCLC)، پستان، کولون و تخمدان دیده میشوند. درمان با داروهای مهار کننده PARP (PARP Inhibitors) مثل Olaparib و Rucaparib در سرطان تخمدان دارای جهشهای BRCA1/2 کاربرد بالینی دارد.
افزایش تعداد کپیهای CD274 بیشتر در سرطانهای پستان، سروگردن و ریه غیر سلول کوچک (NSCLC) دیده میشوند. مطالعات ابتدایی نشاندهنده پاسخ به ایمونوتراپی با استفاده از داروهای Immune checkpoint inhibitors (ICI) مانند Pembrolizumab و Nivolumab در سرطانهای دارای افزایش تعداد کپیهای CD274 میباشد.
جهش در ژن CDKN2A در تشخیص مولکولی تومورهای بدخیم غلاف اعصاب محیطی استفاده میشود. همچنین تأثیر داروهای مهار کننده کینازهای وابسته به سایکلین (CDK4/6) مانند Palbociclib و Abemaciclib درمطالعات کارآزمایی بالینی متعددی بر روی سرطانهای پستان، دهانه رحم و گلیوبلاستوما در حال بررسی میباشند.
وجود جهشهای EGFR به طور شایعی در سرطانهای ریه غیر سلول کوچک (NSCLC)، گلیومای بدخیم، پستان و کولون دیده میشوند. درمان با داروهای مهارکننده EGFR تیروزین کیناز (EGFR TKI) مثل Afatinib، Dacomitinib ،Erlotinib ،Gefitinib و Osimertinib در سرطانهای ریه غیر سلول کوچک (NSCLC) دارای جهشهای خاص EGFR کاربرد بالینی دارد.
ژن ERBB2 پروتئین HER2 را کد میکند. افزایش فعالیت HER2 به صورت افزایش تعداد کپیهای این ژن یا جهشهای فعالکننده در آن به صورت شایعی در سرطان پستان، سرطان ریه غیر سلول کوچک (NSCLC) و سرطان کولون دیده میشود. داروهای مهارکننده HER2 مانند Lapatinib ،Neratininb، Pertuzumab و Trastuzumab در سرطانهای پستان، معده، مری و ریه غیر سلول کوچک که دارای جهشهای فعالکننده HER2 یا افزایش تعداد کپیهای ژن ERBB2 میباشند کاربرد بالینی گستردهای دارند.
وجود جهشهای FGFR3 به طور شایعی در سرطانهای مثانه، ملانوما، ریه غیر سلول کوچک (NSCLC)، پستان و کولون دیده میشود. داروی Erdafitinib در سرطانهای مثانه و مجاری ادراری دارای جهش در ژن FGFR3 استفاده میشود.
وجود جهشهای IDH2 در گلیومای بدخیم و لوکمیا اهمیت دارد. در گلیوما، جهشهای IDH2 با پیش آگهی خوب ارتباط دارند. داروی Enasidenib، در درمان لوکمیای میلویید حاد (AML) دارای جهش در ژن IDH2 استفاده میشود.
وجود جهشهای KIT در نئوپلاسمهای بافت همبند و نرم و همچنین ملانوما و لوکمیا اهمیت دارد. جهشهای KIT در دستهبندی لوکمیای میلویید حاد (AML) و تعیین رژیم درمانی آن استفاده میشوند. همچنین داروهای Dasatinib ،Imatinib ،Nilotinib ،Regorafinib، Sorafenib و Suntinib در درمان تومورهای استرومای دستگاه گوارش (GIST) ، کارسینومای تیموس یا ملانومای دارای جهش در ژن KIT کاربرد دارند.
جهشهای KRAS به طور شایعی در سرطانهای ریه غیر سلول کوچک (NSCLC) و کولون دیده میشوند. سرطانهای کولون دارای جهش در ژن KRAS به داروهای Cetuximab و Panitumumab مقاوم میباشند. همچنین سرطانهای ریه غیر سلول کوچک (NSCLC) به داروهای مهارکننده EGFR تیروزین کیناز (EGFR TKI) مثل Afatinib ،Dacomitinib ،Erlotinib، Gefitinib و Osimertinib مقاوم بوده و پاسخ درمانی مناسبی نمیدهند.
جهشهای MET به طور عمده در سرطان ریه غیر سلول کوچک (NSCLC) دیده میشوند. داروی Crizotinib در تومورهای دارای جهشهایی که منجر به حذف اگزون ۱۴ این ژن میشوند مورد استفاده دارد. همچنین افزایش تعداد کپیهای ژن MET در سرطان ریه غیر سلول کوچک (NSCLC) باعث مقاومت به داروهای مهارکننده EGFR تیروزین کیناز (EGFR TKI) مثل Afatinib ،Dacomitinib ،Erlotinib ،Gefitinib و Osimertinib میشود.
جهشهای NRAS به طور شایعی در ملانوما، لوکمیا و سرطان کولون دیده میشوند. وجود جهشهای NRAS در CMML (Chronic Myelomonocytic Leukemia) و JMML (Juvenile Myelomonocytic Leukemia) با پیش آگهی بد در این سرطانها در ارتباط میباشد. همچنین سرطانهای کولون دارای جهش در ژن NRAS به داروهای Cetuximab و Panitumumab مقاوم میباشند.
محصولات فیوژنی ژنهای NTRK1/2/3 به طور شایعی در سرطانهای ریه غیر سلول کوچک (NSCLC)، کولون، پستان، رحم و ملانوما دیده میشوند. سرطانهای دارای فیوژن هریک از ژنهای NTRK1/2/3 کاندید درمان با داروی Larotrectinib میباشند.
جهشهای NRAS به طور شایعی در ملانوما، لوکمیا و سرطان کولون دیده میشوند. وجود داروهای Dasatinib ،Imatinib یا Suntinib در درمان تومورهای استرومای دستگاه گوارش (GIST) دارای جهش در ژن PDGFRA استفاده میشوند.
جهشهای PIK3CA به طور عمده در سرطان پستان دیده میشوند. ترکیب دارویی Alpelisib و Fulvestrant در تومورهای پستان با رسپتور هورمونی مثبت (ER+) و بدون افزایش کپیهای ژن ERBB2 (HER2-) که دارای جهشهای PIK3CA میباشند، مورد استفاده دارد.
وجود جهشهای IDH1 در گلیومای بدخیم و لوکمیا اهمیت دارد. در گلیوما، جهشهای IDH1 با پیش آگهی خوب ارتباط دارند. داروی Ivosidenib، خط اول درمان در لوکمیای میلویید حاد (AML) دارای جهش در ژن IDH1 میباشد.
گزارش آزمایش Tumor Profiling نوع یک
جهشهای یافت شده در نمونه تومور بررسی شده با آزمایش Tumor Profiling نوع یک با استفاده از پایگاههای داده متعددی از جمله COSMIC ،My Cancer Genome ،CiVIC ،Cancer Hotspots ،PMKB ،ICGC ،MSK-IMPACT و TCGA مورد ارزیابی قرار گرفته و بر اساس دستورالعمل AMP (Association of Molecular Pathologists) طبقهبندی و گزارش میشوند. گزارش آزمایش Tumor Profiling نوع یک علاوه بر تفسیر و طبقهبندی جهشهای یافت شده، اطلاعات کاملی در مورد ژنهای دارای جهش، اهمیت بالینی جهشهای یافت شده و همچنین داروهای توصیه شده بر اساس پروفایل ژنتیکی تومور در اختیار تیم پزشکی بیمار قرار میدهد.

Precision Oncology
بروشورهای Tumor Profiling

دانلود
دستورالعمل جمعآوری نمونه
دانلود
فرم درخواست آزمایش
دانلود
فرم رضایت نامه